Miastènia greu
Informació General
La miastènia greu (MG) és una malaltia neuromuscular poc freqüent que es caracteritza perquè els pacients tenen fatigabilitat i debilitat dels músculs voluntaris.
La debilitat pot afectar qualsevol múscul incloent músculs oculars, de les extremitats i músculs vitals, responsables de la funció respiratòria, de la deglució i de la fonació.
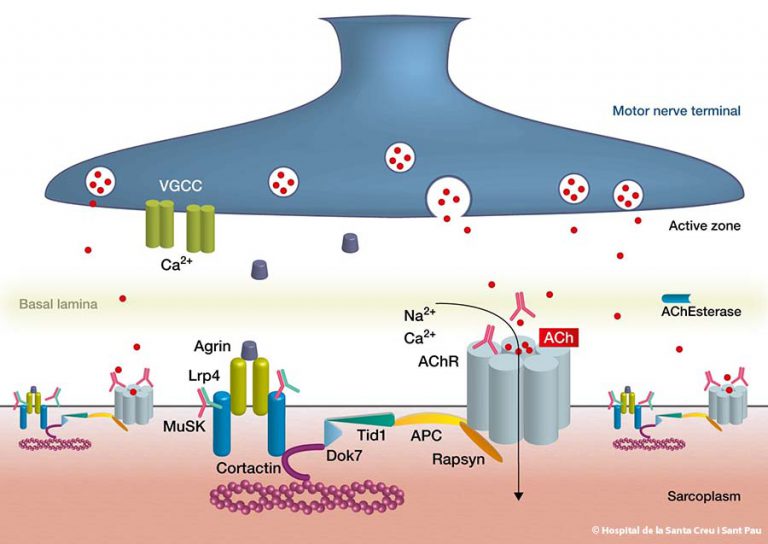
La malaltia és autoimmune, és a dir, es produeixen anticossos enfront de proteïnes pròpies localitzades a la membrana post-sinàptica de la unió neuromuscular (la placa motora). Així doncs, la malaltia no es localitza als nervis ni als músculs pròpiament sinó al lloc d’unió entre nervi i múscul.
La MG és tractable i és per això que ha de ser reconeguda i diagnosticada.
Idealment, els pacients haurien de ser tractats per neuròlegs experts a Miastenia i seguits i controlats pels seus metges de família.
LA MG ÉS UNA MALALTIA DE JOVES?
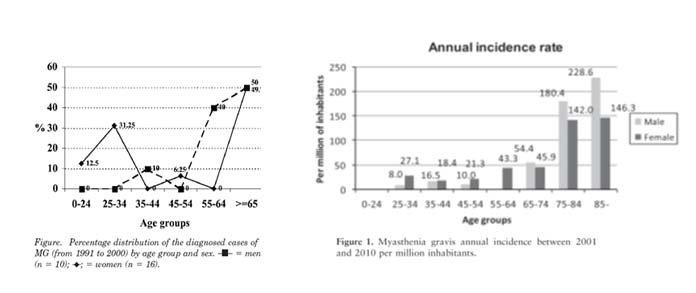
La MG es descrivia clàssicament com una malaltia de pacients joves, entre 15-35 anys i amb un predomini de dones, però actualment se sap que afecta predominantment pacients més grans de 60 anys. En diferents estudis, també al nostre entorn (veure figura) es constata que més del 65% dels pacients nous tenen més de 60 anys. Aquesta és una dada molt important ja que tenim una de les esperances de vida més grans del món. S’ha d’incloure la MG en el diagnòstic diferencial quan la clínica sigui compatible encara que el pacient sigui molt més gran ja que és una malaltia tractable amb una resposta molt bona, sobretot en els ancians.
QUÈ ES CONEIX SOBRE ELS BESTRETS A LA MG
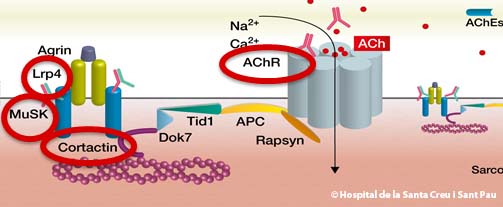
- En més del 80% de casos, La MG és secundària a la presència d’anticossos davant del receptor d’acetilcolina present a la membrana postsinàptica de la unió neuromuscular: MG-RAch+
- Un percentatge dels pacients amb MG-RAch negatius, tenen anticossos davant d’una altra molècula, MuSK, que està localitzada a la mateixa regió de la unió neuromuscular: MG-MuSK+
- El 2012, es va descriure un tercer antigen, LRP4 en un petit nombre de malalts, MG-LRP4+
- El nostre grup ha descrit el 2014 un nou antigen, cortactina (CTTN), en un grup de pacients amb MG ocular o generalitzada IIA, MG-CTTN +
- El 5-7% restant són pacients amb una MG-“Seronegativa”, en què encara avui no s’ha demostrat cap anticòs patogènic, encara que responen als tractaments immunosupressors.
Així doncs la MG és una malaltia heterogènia no només clínicament sinó immunològicament, amb anticossos enfront de com a mínim 4 antígens (RAch, majoritari, MuSK, LRP4, cortactin).
QUINES SÓN LES MANIFESTACIONS CLÍNIQUES?
La principal queixa clínica a la MG és la fatiga muscular que s’acompanya de debilitat muscular. Empitjora al llarg del dia i millora totalment o parcialment amb el repòs. Els símptomes i signes de la miastènia depenen en tot moment de la musculatura implicada que inclou:
- Un 85-90% dels pacients debuten amb afectació de la musculatura ocular, que produeix diplopia (visió doble) i ptosi palpebral unilateral o bilateral, oscil·lant i no necessàriament sempre present.
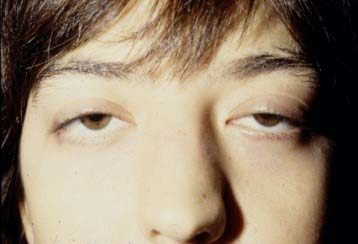
Ptosis palpebral bilateral
- Debilitat de la musculatura facial, sobretot de l’orbicular dels ulls i dels llavis, que confereix una fàscies característica.
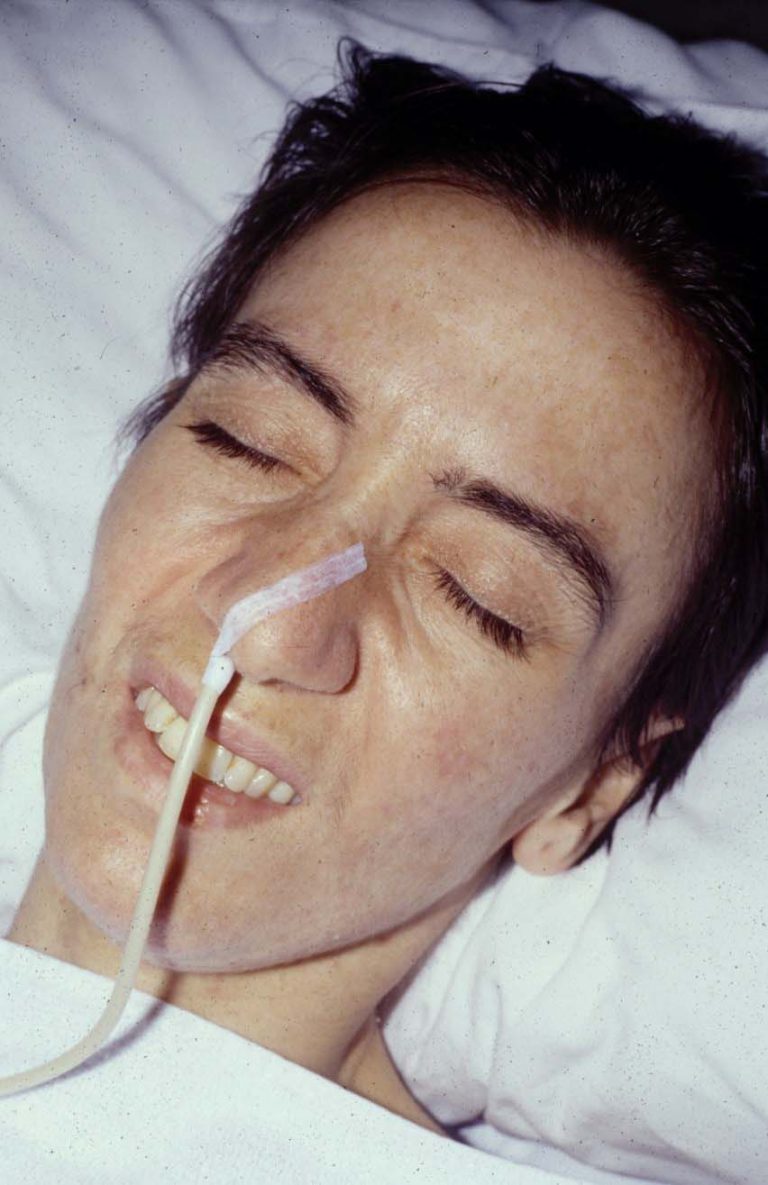
Debilidad facial orbicular ojos y de los labios
- L’afectació de la musculatura cervical provoca debilitat per a l’extensió del coll i en nombroses ocasions la dels músculs masseters claudicació mandibular. Per demostrar la debilitat muscular amb la fatiga, és de gran ajuda sol·licitar al pacient que, en decúbit pron, aixequi el cap fins a 20 vegades (veure fotos en exploració)
- L’afectació de la musculatura bulbar produeix disfàgia, disfonia, disàrtria i dispnea. És la més freqüent en la gent gran i ha de ser reconeguda perquè és la que pot comprometre la vida dels pacients. La clínica és oscil·lant i empitjora quan el pacient repeteix un moviment.
Si la feblesa és important, no es pot objectivar en la història ni en l’exploració aquesta oscil·lació. Davant d’un malalt amb sospita de MG i afectació bulbar amb anticossos antiRAch negatius s’ha de fer l’estudi dels anticossos antiMuSK ja que aquests poden ser positius.
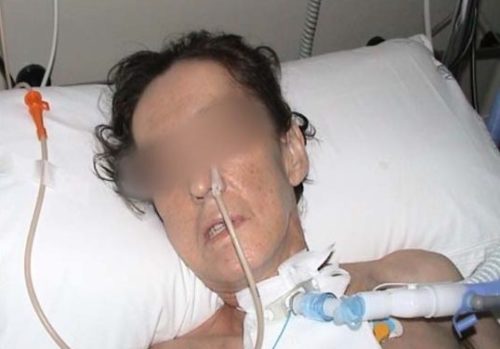
Una situació d’urgència és la crisi miastènica en què es produeix una insuficiència respiratòria aguda; com a conseqüència de l’afectació dels músculs respiratoris. Requereix ingrés hospitalari i de vegades la ventilació mecànica assistida.
- Debilitat i fatigabilitat dels músculs de les extremitats superiors i inferiors sobretot a nivell proximal, tot i que s’han descrit inicis de la malaltia amb debilitat exclusiva dels músculs distals. El pacient presenta generalment dificultat per pujar i baixar escales, manipular objectes per sobre del cap,…
És important plantejar el diagnòstic de M.G no només davant d’aquells pacients que refereixin diplòpia i ptosi palpebral sinó també en aquells malalts, sobretot vells, que tenen disàrtria o disfàgia que varia al llarg del dia. No és infreqüent que se’ls diagnostiqui de malalties molt més prevalents, com ara patologia vascular cerebral.
CLASIFICACIÓN CLÍNICA
L’any 2000 la Myasthenia Gravis Foundation of America (MGFA) va proposar la classificació que més es fa servir en aquest moment.
MG ocular:
- MG – I es reserva per als pacients amb debilitat només de la musculatura ocular.
MG generalitzada:
MG graus II, III i IV s’apliquen a pacients amb clínica generalitzada. Cada grau se subdivideix en grup A si afecta les extremitats i com a grup B si la musculatura predominantment afecta és la bulbar.
- MG-IIA: lleu i de predomini a les extremitats
- MG-IIB: lleu, de predomini bulbar
- MG-IIIA: moderada, de predomini a les extremitats
- MG-IIIB: moderada, de predomini bulbar
- MG-IVA: greu , de predomini a les extremitats
- MG-IVB: greu, de predomini bulbar
- MG-V: es reserva per als pacients en crisi miastènica, que necessiten ventilació
COM ES REALITZA EL DIAGNÒSTIC
El diagnòstic clínic de MG requereix:
- Una història de feblesa muscular i fatigabilitat que empitjoren amb lexercici.
- L’exploració física que demostri la feblesa en diferents grups musculars i l’exclusió d’altres diagnòstics.
Exploració neurològica
L’exploració ha de permetre demostrar l’existència de feblesa en diferents grups musculars en fer moviments repetitius.
A la imatge de l’esquerra s’observa com la pacient fa una flexió normal del coll ia la imatge de la dreta s’objectiva la debilitat dels músculs flexors del coll en repetir-ne la flexió.
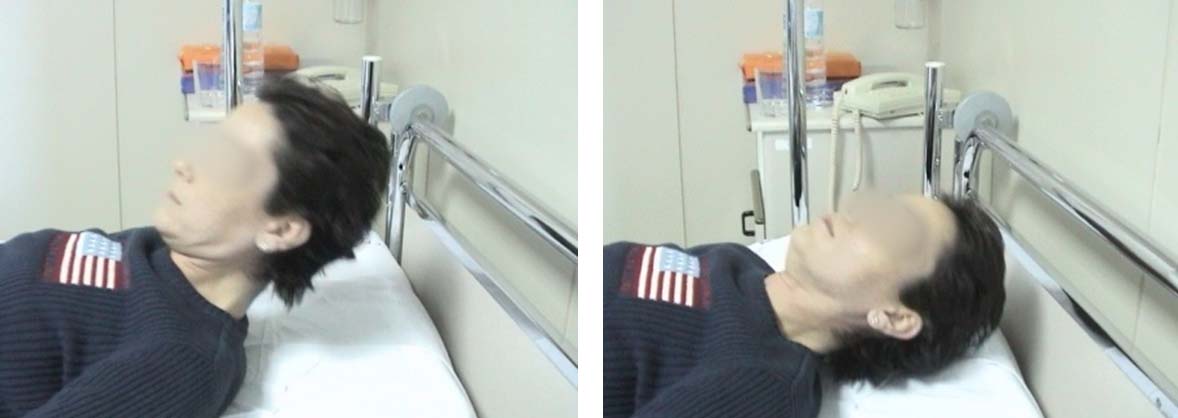
Fatigabilidad muscular cervical con el ejercicio
Davant la sospita clínica, el pacient ha de ser remès al neuròleg especialitzat a Miastenia per realitzar les exploracions complementàries següents:
Test farmacològic
L’administració de clorur d’edrofoni (Tensilón®) (fàrmac anticolinesteràsic) d’ús intravenós (iv) provoca la millora o remissió dels símptomes miastènics en la majoria dels pacients de forma transitòria durant uns miutos. autoanticossos.
Es pot realitzar un test farmacològic amb Mestinon oral, en comptes de Tensilon, sol·licitant al pacient que esperi a la consulta uns 30-40 minuts després d’ingerir 1 comprimit de Mestinon. És útil perquè a més d’observar la tolerància, es pot objectivar amb facilitat el benefici clínic.
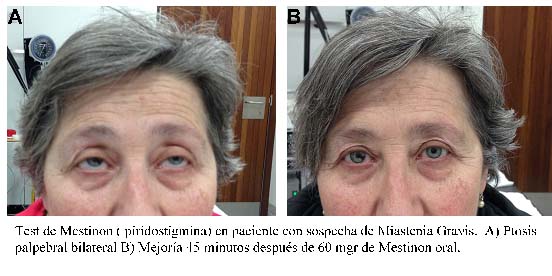
Estudis electrofisiològics
S’utilitzen per demostrar l’alteració en la transmissió neuromuscular a nivell com a causa de la debilitat dels pacients. Els tests que s’utilitzen són l’estimulació repetitiva que és específica però pot ser negativa i l’estudi de fibra aïllada que es reserva per a determinats casos, en què hi ha dubtes diagnòstics perquè és de difícil execució, gens agradable per al pacient i pot ser positiva en altres patologies.
L’estimulació repetitiva es realitza col·locant uns elèctrodes a la superfície de la mà, l’espatlla o el nas i registrant a l’aparell d’EMG el potencial motor obtingut en estimular el nervi de forma repetitiva (el pacient nota que passa un corrent elèctric discretament molest).
La fibra aïllada es realitza inserint una agulla en un múscul, del front o de l’avantbraç, i una segona agulla que novament passa un corrent elèctric. És important la col·laboració del pacient perquè no hi hagi artefactes en l’adquisició dels senyals en aquestes proves.
Estudi d’autoanticossos específics

- Anticossos anti-RACh (Ac.RAch)
Els Ac.RACh són positius fins a un 85% dels pacients amb una miastènia generalitzada i en un 50-60% dels pacients amb miastènia ocular. Són altament específics de MG, encara que s’han descrit a títols baixos en pacients amb timoma, sense clínica de MG i ocasionalment en altres patologies, immunomediades com el lupus i la cirrosi biliar primària. - Anticossos anti-MuSK. (Ac.MuSK)
El 15%-30% dels pacients amb miastènia generalitzada en què no es demostra la presència d’AcRACh tenen un títol positiu d’AcMuSK, que en aquest cas ha de ser superior a 0,05nM. L’especificitat de la prova és del 100% i és excepcional trobar pacients doblement positius de RACh i MuSK. - Anticossos anti-LRP4
Encara no està ben establert el % de pacients seronegatius per a altres anticossos que seran positius per a antiLRP4. S’han trobat positius en diverses malalties immunomediades i, de moment, no són marcadors d’un subgrup de pacients amb miastènia. - Anticossos anti-cortactina CTTN
Aproximadament el 23,7% de pacients amb MG seronegativa i el 9% dels pacients amb MG+RAch tenen aquests anticossos. Els pacients tenen una MG ocular o generalitzada lleu. La determinació daquests anticossos és especialment útil en pacients amb clínica ocular.
Proves complementàries
La MG s’associa amb altres malalties autoimmunes com l’hipertiroïdisme o l’hipotiroïdisme. S’ha de fer l’estudi de la funció tiroïdal així com dels anticossos antiperoxidasa tiroïdal i antitiroglobulina.
Altres malalties que s’associen són el vitiligen, el lupus, l’artritis reumatoidea i l’anèmia perniciosa. En aquests casos és possible detectar anticossos anrtimucosa gàstrica
Estudi d’imatge de l’estafa
En l’abordatge clínic de malalts amb miastènia greu cal descartar sempre l’existència de timoma. Les tècniques d’elecció són TC i/o RM toràciques per determinar si hi ha invasió d’estructures mediastíniques. El percentatge de MG amb timoma és un tema en revisió a nivell internacional en aquests moments. La MG pot ser la primera manifestació del tumor.
DIAGNÒSTIC DIFERENCIAL
El diagnòstic diferencial s’ha de fer amb:
- Esclerosi lateral amiotròfica
- Miopaties mitocondrials
- Distròfia muscular oculofaríngia
- Miopatia per alteració funció tiroïdal
- Paràlisi agudes motores, com el botulisme
- Polineuropatia aguda que afecta els parells cranials i l’encefalopatia de Wernicke
- Síndrome d’Eaton Lambert
- Síndromes miastèniques congènits
- Estats de fatiga emocional, així com la debilitat muscular histèrica o simulada
TRACTAMENT
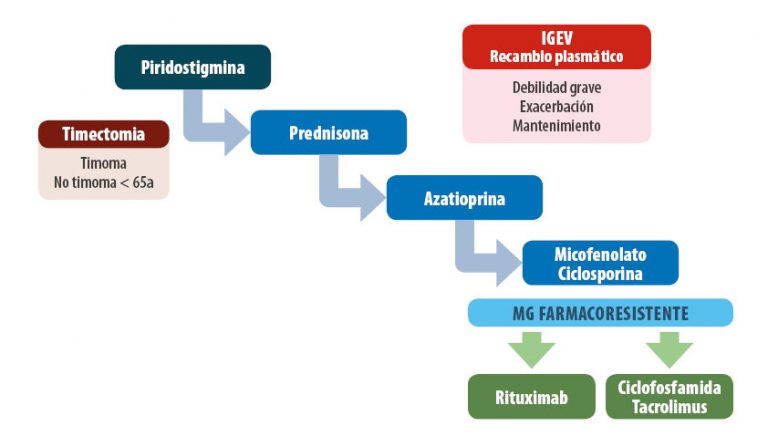
L’objectiu del tractament és aconseguir que el pacient estigui asimptomàtic o amb uns símptomes que li permetin fer vida relativament normal amb els mínims efectes secundaris possibles. Aquest objectiu s’aconsegueix més del 80% dels casos.
El tractament dels pacients amb MG inclou tres aspectes terapèutics diferents:
- Tractament simptomàtic (anticolinesteràsics)
- Timectomia
- Tractament immunològic (immunosupressors)
- Tractament immunomodulador (plasmafèresi i/o Igev)
Tractament simptomàtic amb Anticolinesteràsics
La majoria dels pacients MG-RACh+ responen al tractament en major o menor mesura. No obstant això, menys del 50% dels pacients MG-MuSK+ respon i de fet poden empitjorar.
La piridostigmina (Mestinon 60) és el fàrmac més utilitzat. La dosi inicial oscil·la entre 120 i 300 mg/dia per via oral repartida en dosis de 30-90 mg. L’efecte terapèutic s’inicia als 15-30 minuts i els seus efectes no superen les 4-6 hores. La dosificació és més eficaç si el pacient coneix bé el fàrmac i els seus efectes i flexibilitza les dosis en funció del seu estat de fatigabilitat i horaris.
Els símptomes secundaris es produeixen per un excés d’activitat colinèrgica, i en la majoria de les ocasions són benignes (dolor abdominal, diarrea, rampes i fasciculacions).
Dues precaucions:
- En general han de transcórrer 4-5 hores entre preses de Mestinon
- Si un pacient inicia un empitjorament important i augmenta significativament la dosi de Mestinon, es pot produir una crisi colinèrgica, que s’associa també amb debilitat muscular i s’acompanya de sudoració, hipersialorrea, augment de les secrecions respiratòries, llagrimeig, miosi, nàusees, vòmits i bradicàrdia.
Timectomia
La timectomia es realitzava als pacients amb Miastenia des de l’any 1934 quan es va publicar per primera vegada una millora clínica de la malaltia en operar un pacient amb timoma.
Es considera que la timectomia és beneficiosa en aquells pacients amb MG RAch+, en pacients amb timoma i en menor grau en pacients seronegatius.
El 2016 es va publicar a New England Journal of Medicine un estudi doble cec que demostra que la timectomia juga un paper en el tractament de la Miastènia. En els pacients amb timoma, la timectomia s’ha de realitzar independentment de l’edat del pacient.
En els pacients amb una MG-MuSK, les sèries publicades no han demostrat cap efecte beneficiós.
La tècnica que es fa servir actualment és la toracoscòpia i només es realitza la toracotomia si durant la intervenció es considera necessària.
Tractament immunosupressor
Els immunosupressors han reduït de manera molt important el nombre de crisi i la mortalitat per la malaltia, hi ha encara un nombre de pacients que són resistents als fàrmacs o que aquests els produeixen uns efectes secundaris importants, que afecten la qualitat de vida dels pacients.
Hi ha un consens internacional que el tractament immunosupressor ha d’iniciar-se amb Prednisona. Aquest fàrmac millora més del 50% dels pacients i els seus efectes secundaris es poden minimitzar moltíssim si s’administra en dies alterns i dosis matinal, fet que permet aquesta malaltia. La millora clínica s’obre entre les 3 i les 12 setmanes.
Després o concomitantment s’aconsella utilitzar Aziatoprina o Micofenilat Mofetil per tal de poder reduir al màxim o suprimir la dosi de prednisona. Aquests fàrmacs poden ser utilitzats com a tractament únic en pacients amb una afectació clínica moderada o lleu ja que els efectes clínics es noten entre 6 i 12 mesos d’haver iniciat el tractament.
Si hi ha toxicitat per aquests fàrmacs o els pacients són resistents a aquests fàrmacs, o la debilitat muscular requereix un tractament a més curt termini, el neuròleg pot introduir una sèrie d’immunosupressors, com Ciclosporina, Tacròlim, Ciclofosfamida o Rituximab.
És molt important el seguiment dels pacients per detectar qualsevol dels possibles efectes adversos no només de la prednisona sinó dels immunosupressors (diabetis, hipertensió, osteoporosi, alteració hepàtica o renal,…).
Tractament Immunomodulador
Hi ha dues teràpies, la Plasmafèresi i les Immunoglobulines endovenoses que s’utilitzen quan els pacients amb MG tenen un empitjorament clínic important o estan en crisi miastènica perquè els seus efectes són ràpids però poc duradors. S’utilitza també en aquells pacients recentment diagnosticats, amb debilitat important, que necessiten millorar la debilitat abans que iniciïn el seu efecte els fàrmacs immunosupressors.
FÀRMACS QUE PODEN AFECTAR A LA MIASTÈNIA GRAVIS
S’hi inclou una llista de fàrmacs, dels quals prohibits n’hi ha un (d-penicilamina). La resta de fàrmacs es poden utilitzar, encara que amb la precaució de saber que poden augmentar la debilitat, de manera que, els pacients han d’advertir el metge que pateix MG i els metges han d’advertir els pacients que si empitjoren han de consultar. Per descomptat que la vigilància ha de ser més gran en aquells pacients que ja tenen un cert grau de debilitat. Cal consultar de manera urgent amb el neuròleg sobre l’actitud a prendre, que en alguns casos pot ser la suspensió de la medicació.
Contraindicats:
- D penicilamina
Usar amb gran precaució:
- Telitromicina (usar només si no hi ha cap altra opció possible)
Fàrmacs que augmenten la debilitat a la majoria de pacients:
- Cura i derivats
- Toxina botulínica
- Aminoglucòsids (Gentamicina, Kanamicina, Neomicina, streptomicina, tobramicina)
- Macròlids (Eritromicina, Azitromicina)
- Fluoroquinolones (Ciprofloxacina, Levofloxacina, Norfloxacina)
- Quinina, Quinidina i Procainamida
- Interferó-alfa
- Sals de Magnesi (suplements endovenosos de magnesi)
Fàrmacs que poden augmentar la debilitat en alguns pacients:
- Antagonistes del calci
- Betabloquejants
- Liti
- Contrastos iodats
- Estatines (la relació causal en aquests casos pot ser qüestionable a causa de l’ús estès d’aquests fàrmacs)
ANESTÈSIA GENERAL, ANESTÈSIA LOCAL, INFILTRACIONS
No hi ha, en general, més efectes secundaris amb anestèsia local, que els que es produeixen a la resta de la població. El mateix es pot dir de les infiltracions amb corticoides per problemes locals de tipus tendinitis.
Pel que fa a l’anestèsia general, els pacients han d’advertir al cirurgià i sobretot l’anestesista de la malaltia per que puguin prendre les precaucions necessàries, que en cap cas ha de ser no intervenir el pacient. L’anestèsia general ha de ser administrada en un centre que disposi d’una unitat de seguiment post-quirúrgica o una UCI per si el pacient triga més temps de l’habitual en ser desintubat.
ALIMENTS PROHIBITS
No hi ha cap estudi que demostri que alguns aliments empitjoren la situació clínica dels pacients, excepte aquells que inclouen els compostos que ja estan llistats entre els fàrmacs, com ara l’aigua tònica.
VACUNA CONTRA LA GRIP
Hi ha una controvèrsia sobre l’ús d’aquestes vacunes. Encara que hi ha pacients que han empitjorat la seva clínica, sembla que no passa en la majoria dels casos. El risc es considera important si la vacunació es fa amb microorganismes atenuats (vius) i menys amb microorganismes inactivats (morts). És per això, que es recomana que el metge decideixi si el pacient es beneficiarà de la vacuna per estar immunodeprimit, edat,… i si es produeix un empitjorament clínic el pacient ha de ser derivat al seu neuròleg responsable.
L’EMBARÀS
La Miastènia immunomediada no és hereditària. Pot ser que durant el primer trimestre de l’embaràs hi hagi un empitjorament clínic, però en general durant tot l’embaràs els pacients estan estables i poden ser tractats, si ho necessiten, amb alguns dels esmentats fàrmacs immunosupressors.

